Los corazones requeridos para trasplante son muy escasos, ya que con frecuencia son dañados por enfermedades o por las técnicas propias de resucitación. Pero a lo lejos se vislumbra una esperanza, y es que actualmente los investigadores están buscando diseñar órganos nuevos y completos, con la finalidad de lograr trasplantes en los que no exista riesgo de rechazo por el sistema inmunológico del receptor.
 Sin duda, los trabajos de varios científicos son muy alentadores, como lo son el de Paolo Macchiarini, cirujano en el Instituto de Karolinska en Estocolmo, quien ha trasplantado tráqueas de bioingeniería en varios pacientes y el de Anthony Atala, un urólogo de la Universidad Wake Forest en Winston-Salem, Carolina del Norte, que ha implantado vejigas de bioingeniería en pacientes y está trabajando en la construcción de riñones. Sin embargo en órganos sólidos como el riñón o el pulmón, el desafío es mayor debido a la complejidad de éstos, no así en órganos huecos como la tráquea y la vejiga.
Sin duda, los trabajos de varios científicos son muy alentadores, como lo son el de Paolo Macchiarini, cirujano en el Instituto de Karolinska en Estocolmo, quien ha trasplantado tráqueas de bioingeniería en varios pacientes y el de Anthony Atala, un urólogo de la Universidad Wake Forest en Winston-Salem, Carolina del Norte, que ha implantado vejigas de bioingeniería en pacientes y está trabajando en la construcción de riñones. Sin embargo en órganos sólidos como el riñón o el pulmón, el desafío es mayor debido a la complejidad de éstos, no así en órganos huecos como la tráquea y la vejiga.
Durante más de una década, los biólogos han sido capaces de convertir células madre embrionarias en células del músculo cardíaco en cajas de petri e incluso lograr que mantengan un latido sincrónico por horas con la ayuda de un marcapasos eléctrico externo. No obstante, la compleja estructura del corazón humano está más allá del alcance, incluso, de las máquinas más sofisticadas. Esto es particularmente cierto para las intrincadas redes de capilares que debe suministrar el corazón con oxígeno y nutrientes y eliminar productos de desecho.
Pero la Dra. Taylor, director de la investigación en medicina regenerativa en el Instituto del corazón en Texas en Houston quien ha logrado diseñar el corazón y pulmones de los recién fallecidos, confía en que corazones de bioingeniería podrían en un futuro ser funcionales.
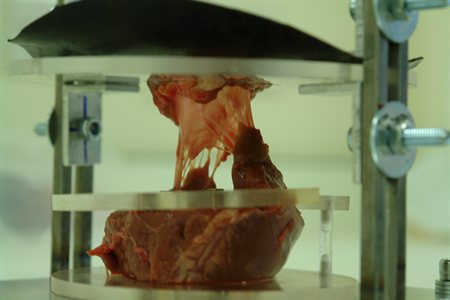
 En donde la estrategia para obtener corazones de bioingeniería es bastante simple en principio. Harald Ott, cirujano e investigador de medicina regenerativa, explica el método: El corazón fresco se encuentra en una cámara de vidrio y plástico suspendido por tubos de plástico. El primer paso es eliminar todas las células del órgano muerto (ni siquiera tiene que ser de un ser humano; los corazones de cerdos son muy prometedores), este proceso es conocido como descelularización y consiste en inyectar detergente a través de la aorta del corazón para lograr que se disperse a través de todos los conductos. Al cabo de una semana aproximadamente el detergente habrá eliminado lípidos, DNA, proteínas solubles, azúcares y casi todo el material celular del corazón, dejando solamente una delgada malla de colágeno y otras proteínas estructurales (matriz extracelular). Posteriormente viene la repoblación con células madre (stem cells) que se diferenciarán en células cardíacas, inmunológicamente emparentadas con las que el paciente requiere.
En donde la estrategia para obtener corazones de bioingeniería es bastante simple en principio. Harald Ott, cirujano e investigador de medicina regenerativa, explica el método: El corazón fresco se encuentra en una cámara de vidrio y plástico suspendido por tubos de plástico. El primer paso es eliminar todas las células del órgano muerto (ni siquiera tiene que ser de un ser humano; los corazones de cerdos son muy prometedores), este proceso es conocido como descelularización y consiste en inyectar detergente a través de la aorta del corazón para lograr que se disperse a través de todos los conductos. Al cabo de una semana aproximadamente el detergente habrá eliminado lípidos, DNA, proteínas solubles, azúcares y casi todo el material celular del corazón, dejando solamente una delgada malla de colágeno y otras proteínas estructurales (matriz extracelular). Posteriormente viene la repoblación con células madre (stem cells) que se diferenciarán en células cardíacas, inmunológicamente emparentadas con las que el paciente requiere.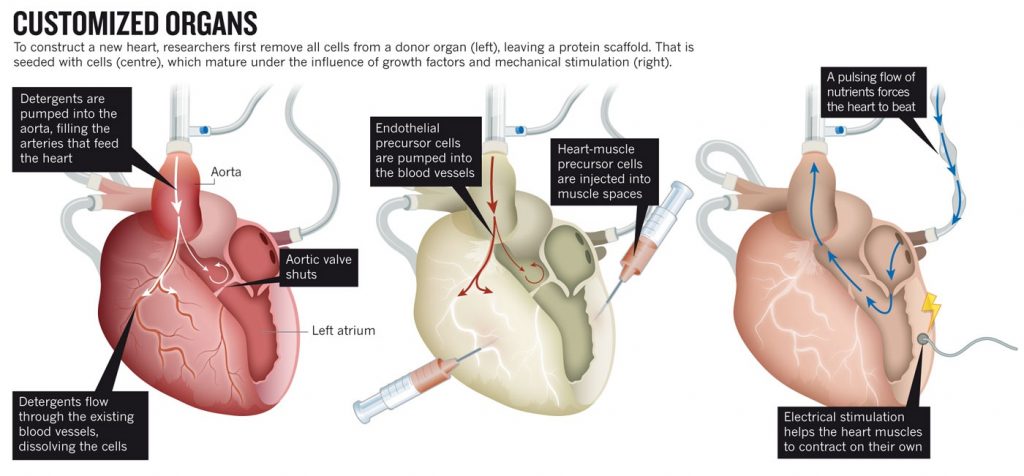
Aunque sencillo en principio, tiene la desventaja de que una cantidad inadecuada de detergente puede inducir a la pérdida de material importante o a la presencia de material no deseado. Además de que la repoblación con células madre implica grandes cantidades de éstas debido al gran tamaño que tiene el corazón, y otro problema es que cuando estos cardiomiocitos comiencen a ser funcionales no solo necesitarán medios oxigenados o factores de crecimiento, sino también la rigidez y la tensión mecánica. Así que los investigadores también enfrentan una gran batalla por imitar los cambios de frecuencia cardíaca y presión arterial o la presencia de fármacos. Los investigadores han tratado de compensar esta situación utilizando biorreactores que imitan el latido.
El reto final y más difícil es colocar el corazón de ingeniería genética en un animal vivo y mantenerlo latiendo por un largo tiempo. Pero aunque los investigadores pueden alimentar a los órganos con sangre y hacer que vencieron por un tiempo, ninguno de los corazones ha sido capaz de soportar la función de bombeo de sangre. Los investigadores necesitan demostrar que un corazón tiene mucho más capacidad de funcionar antes de que se pueda trasplantar en un animal más grande que una rata.
(Tomado de Nature)
El conocimiento profundo que se adquiera gracias a toda esta investigación, sin duda, ayudará a mejorar las terapias de tratamiento en enfermedades del corazón y quizá, tal vez algún día permita cumplir el sueño de tener órganos de bioingeniería disponibles para trasplantes, sin embargo no debemos olvidar que las técnicas de nuestra mortalidad sólo nos permitirán reutilizar lo que ya ha sido creado.